2026 – Senaryo 2 (MEB)

SORU 1

SORU 2 – A

SORU 2 – B

SORU 2 – C

SORU 3
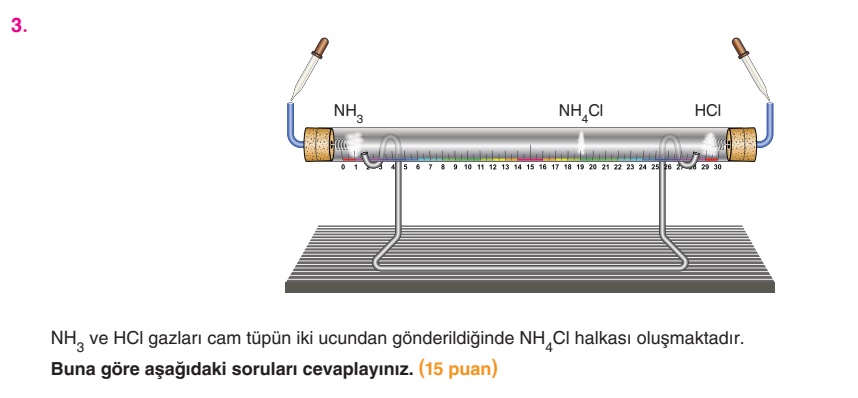
- Bu deney gazların hangi özelliğini göstermektedir?
- ……………………………………………………………………………………………………
- Gazlarını buluşma noktası için ne söylenebilir?
- ……………………………………………………………………………………………………
SORU 4

SORU 5

SORU 6

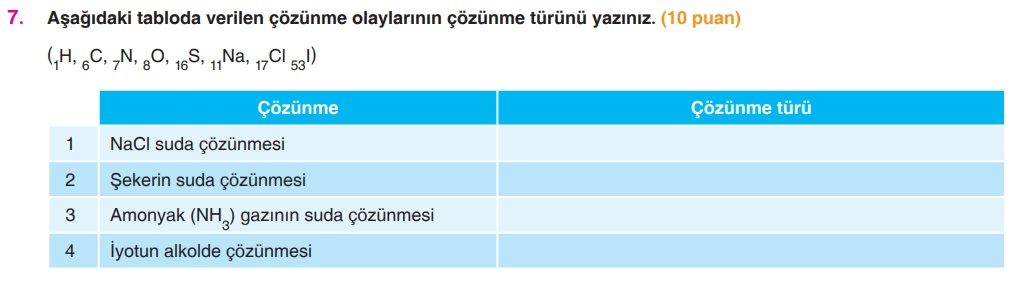
SORU 7
SORU 8

2026 – Senaryo 3 (MEB)

SORU 1
0oC sıcaklıkta ve 2 atm basınç yapan ideal bir gazın hacmi 5,6 litredir.
Bu kapta bulunan gazın mol sayısı kaçtır? (R=22,4/273)
SORU 2
90 cm uzunluğundaki cam boru ile bağlanmış kaplarda bulunan SO2 ve CH4 gazları ile kurulmuş düzeneğin görseli aşağıda verilmiştir.

Musluklar aynı anda açılarak gazların ilk karşılaştığı noktalar kaydediliyor. Buna göre aşağıdaki soruları cevaplayınız.
I) Gazların sıcaklıkları aynı olduğunda SO2 gazının bulunduğu uçtan 30 cm uzaklıkta karşılaşıyorlar.
SO2 gazının mol kütlesi ile CH4 gazının mol kütlesini kıyaslayınız.
II) Gazların tam ortada karşılaşması için sıcaklıkları arasındaki ilişki ne olmalıdır?
SORU 3
4,1 litrelik kapalı bir kapta 127oC sıcaklıkta bulunan 0,5 mol X gazının basıncı kaç atm’dir? (R=82/1000)
SORU 4
Aynı sıcaklıkta bulunan X ve Y gazlarından, X gazının mol kütlesi 4 g/mol, Y gazının mol kütlesi ise 64 g/mol’dür. Buna göre şu soruları cevaplandırınız:
I) Gazların yayılma hızlarını karşılaştırınız.
II) Bu gazların yayılma hızlarını eşitlemek için X ve Y gazlarının sıcaklıkları nasıl değiştirilebilir? Nedenini açıklayınız.
SORU 5
Çözünme olayı gerçekleşirken meydana gelen 3 temel aşamayı sırasıyla yazınız.
SORU 6
Aşağıdaki madde çiftlerinin birbiri içinde çözünüp çözünmeyeceğini “ÇÖZÜNÜR” veya “ÇÖZÜNMEZ” şeklinde belirtiniz.
| Madde Çiftleri | Çözünme Durumu |
| H2O – C6H6 | |
| H2O – HF | |
| NaCl – CH4 | |
| O2 – CO2 |
SORU 7
Aşağıda verilen çözünme örneklerini “İYONİK ÇÖZÜNME” ya da “MOLEKÜLER ÇÖZÜNME” olarak sınıflandırınız.
| Madde Çiftleri | Çözünme Türü |
| Şekerin suda çözünmesi | |
| Yemek tuzunun suda çözünmesi | |
| Metil alkolün (CH3OH) suda çözünmesi | |
| Hidroklorik asidin suda çözünmesi |
2026 – Senaryo 3 (MEB)

SORU 1
Standart koşullarda aşağıdaki 11,2 litrelik sabit hacimli kapta bulunan 8 gram CH4 gazı 1 atm basınç yapmaktadır. Kaba aynı sıcaklıkta bir miktar He gazı eklendiğinde kabın son basıncı 2 atm olarak ölçülüyor. (H: 1, He: 4, C: 12)
Buna göre;
I) Kaba eklenen He gazı kaç gramdır?
II) Kaptaki gaz yoğunluğu başlangıca göre kaç katına çıkmıştır?
Soru 2

SORU 3
Aşağıdaki şekilde verilen cam borunun uçlarında 27oC sıcaklıktaki He ve SO2 gazları bulunan kaplar bağlanmıştır. Musluklar aynı anda açılarak gazların ilk karşılaştığı nokta kaydediliyor.

Buna göre;
I) Gazların ilk karşılaştığı noktanın hangi gaza daha yakın olacağını nedeni ile açıklayarak yazınız. (He:4 g/mol, SO2:64 g/mol)
II) Gazların tam orta noktada karşılaşmasını sağlamak için gazlardan birinin sıcaklığına nasıl etki yapılabileceğini nedenini yazarak açıklayınız.
SORU 4
Şehir gazı kaçaklarının tespit edilmesi için kokusuz olan doğal gaza neden ağır kokulu maddeler eklenir? Bu durum gazların hangi yayılma özelliği ile ilgilidir? Kısaca açıklayınız.
SORU 5
Yanda verilen madde çiftlerinin birbiri içerisinde homojen bir karışım (çözelti) oluşturma durumunu “ÇÖZÜNÜR” veya “ÇÖZÜNMEZ” şeklinde yazarak iki durum için de tanecikler arası kurulacak etkileşim türünü yazınız.
Madde Çifti | Çözünme Durumu | Tanecikler Arası Etkileşim Türü |
| H2O – C6H6 | ||
| Br2 – CCl4 | ||
| NH3 – H2O | ||
| MgO – H2O | ||
| HCl – H2O | ||
| CaBr2 – CH4 |
SORU 6
Çözünme sürecinde temel anlamda üç basamağın gerçekleşmesi gerekir.
Bu basamakları yazarak hidratasyon ve solvatasyon olaylarına birer örnek veriniz.
SORU 7
Aşağıda çözünme denklemleri verilen tepkimeleri tablodaki uygun yerlere işaret (X) koyarak “İYONİK veya MOKELÜLER” ve “FİZİKSEL veya KİMYASAL” olarak sınıflandırınız.
a) MgCl2(k) + H2O(s) –> Mg2+(suda) + 2Cl–(suda)
b) C2H5OH(s) + H2O(s) –> C2H5OH(suda)
c) CO2(g) + H2O(s) –> H+(suda) + HCO3–(suda)
d) N2O5(g) + H2O(s) –> 2HNO3(suda)
| İYONİK | MOLEKÜLER | FİZİKSEL | KİMYASAL | |
| a) | ||||
| b) | ||||
| c) | ||||
| d) |