ETKİLEŞİM (KİMYA 10) → 2. Bölüm
DERS
KİMYA 10
1. TEMA
ETKİLEŞİM
KONU
2. BÖLÜM:
1.2. Gazlar
1.2.1. Gazların Özellikleri ve Gaz Yasaları
Gazların Genel Özellikleri
- Yayılma:
- İçinde bulundukları kabın her yerine yayılırlar.
- Bu yüzden kabın hacmini kaplarlar şeklini alırlar.
- Sıkışma ve genleşme:
- Kimyasal türleri arasında büyükboşluklar vardır.
- Bu yüzden, sıkıştırılabilirler.
- Isıtıldıklarında oldukça geneleşebilirler.
- Kimyasal türleri arasında büyükboşluklar vardır.
- Kimyasal türleri; titreşim, öteleme ve dönme hareketi yaparlar.
- Gazların bir “gaz basıncı” vardır.
- Kaplarının her yerine eşit basınç yapar.
- Gazlar, maddenin en düzensiz hâlidir.
- Maddenin, enerjisinin en yüksek olduğu halidir.
- Basınç, hacim, sıcaklık ve miktar; gazları tarif etmek için kullanılan temel özelliklerdir.
Suyun Gaz Hali
Gazların Genel Özellikleri


Gazların 4 Temel Özelliği
1. Basınç – P
- Tanım: Birim yüzeye etki eden kuvvete basınç denir.
- Sembolü: Basınç; P harfi ile gösterilir.
- Birimi: Basıncın birimi; atm (atmosfer) veya cmHg veya Torr‘dur.
- 1 atm = 76 cmHg = 760 mmHg = 760 Torr
- 1 atm = 101 325 Pa (yaklaşık 105 Pa)
- 1 atm = 1,01325 Bar (yaklaşık 1 Bar)
- Hava da bir gaz karışımıdır ve bir basıncı vardır.
- Hava basıncına, atmosfer basıncı veya hava basıncı veya dış basınç denir.
- Hava basıncı; Pdış veya P0 veya Phava şeklinde gösterilir.
- Normal Koşullar:
- 0oC sıcaklık,1 atm basınç demektir.
- Oda Koşulları veya Standart Koşullar :
- 25oC sıcaklık, 1 atm basınç demektir.
- Açık hava basıncı barometre ile
- Kapalı kaplardaki gaz basıncı ise manometre ile ölçülür.
1. Basınç – P
- Gazlar 2 tür kap içinde saklanır. Bunlar;
- Sabit hacimli kaplar
- Sabit basınçlı kaplar
- Sabit basınçlı kaplar şunlardır:
- İdeal pistonlu kap
- İdeal elastik balon
- Sabit hacimli kap örnekleri şunlardır:
- Düdüklü tencere
- Kavanoz
- Şişe
Örnek:

Buna göre şekilde verilen kaplardan hangileri sabit basınçlı kaplardır?
A) Yalnız I
B) Yalnız II
C) Yalnız III
D) II ve III
E) I, II ve III
Gazların 4 Temel Özelliği
Örnek:
a) 0,5 atm = ? mmHg
b) 190 Torr = ? atm
c) 114 cmHg = ? atm
Yukarıda verilen birimleri, karşısındaki birime çeviriniz.
Gazların 4 Temel Özelliği
2. Hacim – V
- Tanım: Maddenin boşlukta kapladığı yere hacim denir.
- Sembolü: Hacim; V harfi ile gösterilir.
- Birimi: Hacmin birimi; L veya m3 ve katlarıdır.
- 1 L = 1 dm3 = 1000 cm3 = 1000 mL
- 1 cm3 = 1 mL
- Bir gazın hacmi demek bulunduğu kabın hacmi demektir.
- Standart koşullarda:
- 1 mol gaz, her zaman, 24,5 L hacim kaplarken
- Normal koşullarda:
- 1 mol gaz, her zaman, 22,4 L hacim kaplar.
Gazların 4 Temel Özelliği
3. Miktar – n
- Gazların miktarı genellikle mol sayısı olarak verilir ya da istenir.
- Tanım: 1 mol kimyasal tür, 6,02×1023 tanedir.
- Sembolü: Mol sayısı; n harfi ile gösterilir.
- Birimi: Mol sayısının birimi; mol‘dür.
- 6,02×1023 sayısına Avogadro sayısı denir ve N, NA veya N0 sembollerinden biri ile gösterilir.
- Normal koşullarda 1 mol gaz 22,4 L hacim kaplar.
- Standart koşullarda 1 mol gaz 24,5 L hacim kaplar.
- 1 mol gaz her zaman mol ağırlığı (MA) kadar gram gelir.
Gazların 4 Temel Özelliği
4. Sıcaklık – T
- Tanım: Bir maddenin ortalama kinetik enerjisinin göstergesidir.
- Gazların sıcaklıkları, Kelvin ya da Celcius cinsinden verilecek ya da sorulacaktır.
- Sembolü: Kelvin cinsinden sıcaklık T harfi ile; santigrad (celsius) derece cinsinden sıcaklık ise t harfi ile gösterilir.
- Birimi: Kelvinin biri K, santigrad derecenin birimi oC’dir.
T = t + 273
- Sıcaklıkları eşit olan gazların ortalama kinetik enerjileri de eşittir.
Gaz Yasaları
Gaz Yasası Nedir?
- Gazların bir özelliği değiştiğinde, diğer özelliğinin bundan nasıl etkilendiğini açıklayan kurallara gaz yasası denir.
- Dört temel gaz yasası vardır:
- Boyle Yasası (P – V ilişkisi)
- Charles Yasası (V – T ilişkisi)
- Gay-Lussac Yasası (P – T ilişkisi)
- Avogadro Yasası (V – n ilişkisi)
Doğru Orantılı İki Büküklük
X artarsa Y de artar.

Ters Orantılı İki Büyüklük
Y artarsa X azalır.
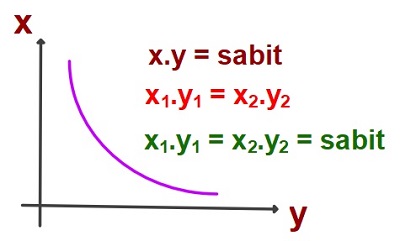
Hatırla, Çok Lazım Olacak!!!
Gaz Yasaları
1. Boyle Yasası (P – V İlişkisi)
- Kanun: Sıcaklığı ve miktarı sabit bir gazın, basıncı ile hacmi doğru orantılıdır (Sıkışan gaz büzüşür):
- Bu kanunun formülü şöyledir:

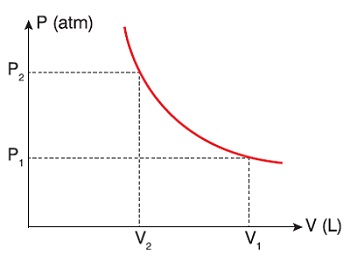
Gaz Yasaları
Örnek:
Sabit sıcaklıkta ve ideal pistonlu bir kapta bulunan bir gazın hacmi 12 L, basıncı 0,5 atm’dir.
Bu gazın basıncının, 1,5 atm olması için, hacminin kaç Litreye getirilmesi gerekir?
Gaz Yasaları
2. Charles Yasası (V – T İlişkisi)
- Kanun: Basıncı ve miktarı sabit bir gazın, hacmi ile sıcaklığı doğru orantılıdır:
- Bu kanunun formülü şöyledir:

Charles Yasası
Gaz Yasaları
Örnek:
Sabit basınçlı, sürtünmesiz pistonlu kapta bulunan bir gazın; sıcaklığı 400 K, hacmi 3 L’dir.
Gazın hacminin 4,5 Litre olması için, sıcaklığının kaç Kelvin’e getirilmesi gerekir?
Gaz Yasaları
3. Gay-Lussac Yasası (P – T İlişkisi)
- Kanun: Hacmi ve miktarı sabit bir gazın, basıncı ile sıcaklığı doğru orantılıdır:
- Bu kanunun formülü şöyledir:

Charles Yasası
Gaz Yasaları
Örnek:
Sabit hacimli bir kapta, belirli miktardaki bir gazın, basıncı 6 atm ve sıcaklığı 600 K’dir.
Gazın sıcaklığı 200 K’e düşürülürse, basıncı kaç atmosfer olur?
Gaz Yasaları
4. Avogadro Yasası (V – n İlişkisi)
- Kanun: Basıncı ve sıcaklığı sabit bir gazın, hacmi ile mol sayısı doğru orantılıdır:
- Bu kanunun formülü şöyledir:

Örnek:
Sabit basınçlı, 12 L’lik bir kapta, 4 mol gaz vardır.
Sıcaklık sabitken, kaba 4 mol daha gaz konulursa, kabın son hacmi ne olur?
Bileşik Gaz Yasası
Bileşik gaz yasası, şimdiye kadar gördüğümüz 4 gaz yasasının birleşmiş halidir. Formülü şudur:
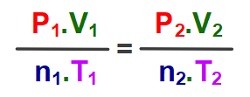
Gaz yasalarına ait bütün sorular, bileşik gaz yasası ile de çözülebilir.
Örnek:
Belli bir miktar gazın, hacmi yarıya indirilip, mutlak sıcaklığı 4 katına çıkarılıyor.
Buna göre, bu gazın basıncı nasıl değişir?
Örnek:
Sabit basınç ve sıcaklıkta, 4 g H2 gazı 60 L hacim kaplamaktadır.
Aynı şartlarda 32 gram SO2 gazı kaç Litre hacim kaplar?
(H: 1 g/mol, S: 32 g/mol, O: 16 g/mol)
Örnek:

Şekil, He ve O2 gazlarından oluşan bir gaz karışımı içeren sabit hacimli bir kaba aittir.
Buna göre bu gaz karışımı için;
I) Homojen bir karışımdır.
II) Gazların sıcaklıkları eşittir.
III) Gazların ortalama kinetik enerjileri eşittir.
yargılarından hangileri doğrudur?
A) Yalnız I
B) Yalnız II
C) Yalnız III
D) II ve III
E) I, II ve III
Örnek:
İdeal pistonlu bir kapta, 273o C sıcaklıkta 8,8 gram CO2 gazı bulunmaktadır. Bu kaba aynı sıcaklıkta bir miktar He gazı eklendiğinde kabın hacmi başlangıç hacminin 3 katına çıkmaktadır.
Daha sonra sistemin sıcaklığı 0oC’ye düşürülürse, son durumda He gazının kısmi basıncının toplam basınca oranı ve kaptaki toplam hacim () aşağıdakilerden hangisinde doğru verilmiştir?
(C: 12, O: 16, He: 4, , Dış basınç: 1atm)

1.2. Gazlar
1.2.1. Gazların Özellikleri ve Gaz Yasaları
Bitti 🙁