ETKİLEŞİM (KİMYA 10) → 1. Bölüm
DERS
KİMYA 10
1. TEMA
ETKİLEŞİM
KONU
1. BÖLÜM:
1.1. Kimyasal Tepkimeler
1.1.2. Kimyasal Tepkime Türleri
10.1.2 Kimyasal Tepkime Türleri
- Kimyasal tepkime türlerinin bazıları şunlardır:
- Çökelme tepkimeleri
- İndirgenme-yükseltgenme tepkimeleri
- Asit-baz tepkimeleri
1. Çökelme Tepkimeleri
AgNO3(suda) + NaCl(suda) → AgCl(k) + NaNO3(suda)
- Suda çözünmüş maddeler tepkimeye girer, tepkime sonucunda suda çözünmeyen katı bir madde oluşur.
- Dibe çökerek ayrılan katıya çökelek (çökelti), gerçekleşen tepkimeye de çökelme tepkimesi denir.
10.1.2 Kimyasal Tepkime Türleri
1. Çökelme Tepkimeleri
AgNO3(suda) + NaCl(suda) → AgCl(k) + NaNO3(suda)
- İyonik bileşikler suda iyonlarına ayrıştığı için bu tepkime aşağıdaki gibi yazılır:
Ag+(suda) + NO3–(suda) + Na+(suda) + Cl–(suda) → AgCl(k) + Na+(suda) + NO3–(suda)
Seyirci iyonlar:
- Na+ ve NO3– iyonları tepkimenin her iki tarafında da çözeltide kaldığı için bu iyonlara seyirci iyonlar (net tepkimede bulunmayan) denir.
Net iyon denklemi:
- Her iki taraftaki seyirci iyonlar sadeleştirildiğinde net iyon denklemi elde edilir:
- Ag+(suda) + Cl–(suda) → AgCl(k)
10.1.2 Kimyasal Tepkime Türleri
1. Çökelme Tepkimeleri
İkili Yer Değiştirme Tepkimesi

- Bir çok çökelme tepkimesi genellikle ikili yer değiştirme tepkimesi şeklinde gerçekleşir.
- Bu tepkimelerde bileşiklerin iyonları karşılıklı olarak yer değiştirir.
Örnek Tepkime
2KI(suda) + Pb(NO3)2(suda) → Pbl2(k) + 2KNO3(suda)
10.1.2 Kimyasal Tepkime Türleri
1. Çökelme Tepkimeleri
Çevremizden Bazı Çökelme Tepkimeleri
- Çevremizden bazı çökelme tepkimeleri:
- Çaydanlıkların kireçlenmesi
- Sarkıt, dikit ve travertenlerin oluşumu
- Böbrek ve safra taşlarının oluşması



10.1.2 Kimyasal Tepkime Türleri
2. İndirgenme-Yükseltgenme (Redoks) Tepkimeleri
- Mutlaka elektron alan ve elektron veren atomlar vardır.
- Alınan-verilen elektron sayısı daima eşittir.
Örnek:
2Mg(k) + O2(g) → 2MgO(k)

- Nötr magnezyum atomları 2’şer elektron vermiş ve yükleri +2’ye yükselmiştir.
- Elektron verme olayına yükseltgenme denir.
- Yükseltgenen atomlar indirgendir.
- Nötr oksijen atomları 2’şer elektron almış ve yükleri -2’ye inmiştir.
- Elektron alma olayına indirgenme denir.
- İndirgenen atomlar yükseltgendir.
10.1.2 Kimyasal Tepkime Türleri
2. İndirgenme-Yükseltgenme (Redoks) Tepkimeleri
Yüklerin Bulunması
- Kimyasal maddelerin toplam yükü sembol ya da formüllerinin sağ üst köşesinde verilir.
- Bileşiklerde yer alan bütün atomların bir yükü vardır fakat verilmez.
- Bu yükler ezbere bilinmelidir.
- Element halindeki maddelerin yükü verilir, verilmediyse yükleri sıfır demektir.
Bazı Kimyasalların Bileşiklerindeki Yükleri
- Li1+, Na1+, K1+, Ag1+, Cu+, NH41+
- Be2+, Mg2+, Ca2+, Fe2+, Sn2+, Pb2+, Zn2+, Co2+, Cu2+
- Al3+, Fe3+, Co3+
- Pb4+, Sn4+
- F1-, Cl1-, Br1-, CN1-, OH1-, NO31-, ClO41-
- O2-, S2-, SO32-, SO42-, CO32-
- N3–, PO43-
- C4-
10.1.2 Kimyasal Tepkime Türleri
2. İndirgenme-Yükseltgenme (Redoks) Tepkimeleri
Örnek
Na + H2O → NaOH + 1/2H2
tepkimesi için aşağıdaki soruları cevaplandırınız.
- Yükseltgenen atom:
- İndirgenen atom:
- Yükseltgen atom:
- İndirgen atom:
10.1.2 Kimyasal Tepkime Türleri
2. İndirgenme-Yükseltgenme (Redoks) Tepkimeleri
Bazı Redoks Tepkimelerinin Sembolik Gösterimi
- Tepkimede yüksüz bir element varsa tepkime redokstur:
3O2 + 2Fe → 2Fe2O3
2AgNO3(suda) + Cu(k) → Cu(NO3)2(suda) + 2Ag(k)
CH4 + O2 → CO2 + H2O
Çevremizden Bazı Redoks Tepkimeleri
- Yanma tepkimeleri
- Metallerin tuz çözeltileriyle olan tepkimeleri
- Pillerin çalışması
- Asitlerin metallerle tepkimesi
- Ağartıcıların kumaşın rengini değiştirmesi
- Fotosentez ve solunum
10.1.2 Kimyasal Tepkime Türleri
2. İndirgenme-Yükseltgenme (Redoks) Tepkimeleri
Tekli Yer Değiştirme Tepkimesi
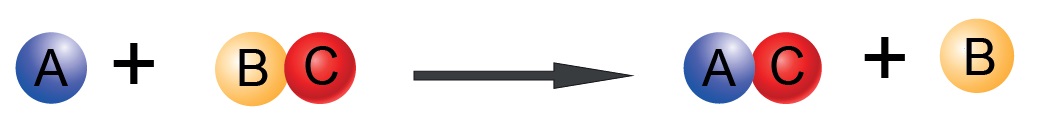
- Bir çok redoks tepkimesi genellikle tekli yer değiştirme tepkimesi şeklinde gerçekleşir.
- Bu tepkimelerde bir element bir bileşiğin iyonu ile yer değiştirir.
Örnek Tepkime
Mg(k) + 2HCl(suda) → MgCl2(suda) + H2(g)
10.1.2 Kimyasal Tepkime Türleri
3. Asit-Baz Tepkimeleri
Arrhenius Asit-Baz Tanımı
- Arrhenius’a göre asit-bazlar şöyle tanınır:
- Asit: Suda çözündüğünde çözeltiye H+ (hidrojen) veya H3O+ (hidronyum) iyonu verebilen bileşiklere denir.
- Baz: Suda çözündüğünde çözeltiye OH– (hidroksit) iyonu verebilen bileşiklere denir.
Örnek:
I) HCl(s) → H+(suda) + Cl–(suda)
II) NaOH(k) → Na+(suda) + OH–(suda)
III) HClO4(s) → H+(suda) + ClO4–(suda)
IV) Ca(OH)2(k) → Ca2+(suda) + 2OH–(suda)
V) NH3(suda) + H2O(s) ⇄ NH4+(suda) + OH–(suda)
Yukarıda verilen çözünme tepkimelere bakarak, maddeleri asit ve baz olarak sınıflandırınız.
10.1.2 Kimyasal Tepkime Türleri
3. Asit-Baz Tepkimeleri
- Asit baz tepkimelerine nötralleşme tepkimeleri de denir.
- Çünkü su da oluşur.
Asit + Baz → Tuz + Su
(Nötrleşme tepkimesi)
Örnekler
- NaOH(suda) + HCl(suda) → NaCl(suda) + H2O(s)
- 2NaOH(suda) + H2SO4(suda) → Na2SO4(suda) + 2H2O(s)
Net İyon Denklemi
H+(suda) +OH–(suda) → H2O(s)
- Suyun oluşumu hem nötralleşme tepkimesidir, hem de net iyon denklemidir:
- Oluşan tuz genellikle suda çözünmeye devam eder.
- Tuzun iyonları bu yüzden seyirci iyonlardır.