ÇEŞİTLİLİK (KİMYA 10) → 1. Bölüm
DERS
KİMYA 10
2. TEMA
ÇEŞİTLİLİK
KONU
2.1. Çözeltiler
2.1.2. Maddelerin Birbiri İçindeki Çözünebilirliği
Hangi Maddeler Birbirinde Daha İyi Çözünür?
Benzer benzerde iyi çözünür
- Polar maddeler polar çözücülerde iyi çözünür.
- Apolar maddeler apolar çözücülerde iyi çözünür.
Polar kimyasal türler:
- H2O : Su
- NaCl : Yemek tuzu
- KCl : Postasyum klorür
- NH3 : Amonyak
- C12H22O11 : Çay şekeri
- CH3OH : Metanol
- C2H5OH : Etanol
- HF: Hidrojen florür
- NaOH : Sodyum hidroksit
- CH3COOH : Asetik asit
Apolar kimyasal türler:
- C6H6 : Benzen
- CCl4 : Karbon tetraklorür
- I2 : İyot
- C10H8 : Naftalin
- C6H14 : Hekzan
Örnek:
Aşağıda verilen madde çiftlerinden hangisinin bir çözelti oluşturması beklenmez?
A) H2O ve NaCl
B) CCl4 ve I2
C) H2O ve CH3OH
D) C6H6 ve H2O
E) C10H8 ve C6H6
Çözücü-Çözünen Etkileşimleri
Örnek:
Aşağıdaki tabloyu doldurunuz:
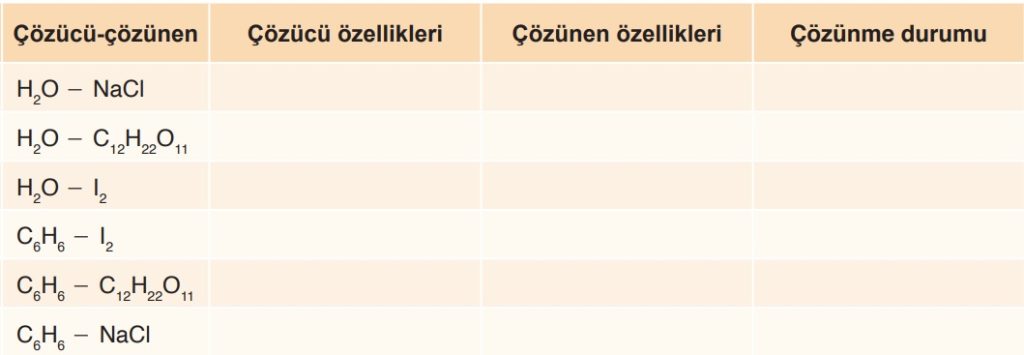
Çözücü-Çözünen Etkileşimleri
- Çözeltilerde; çözücü ile çözünen maddenin kimyasal türleri arasında zayıf etkileşimler kurulur.
- Zayıf etkileşimler nokta noktalarla (……..) gösterilir.

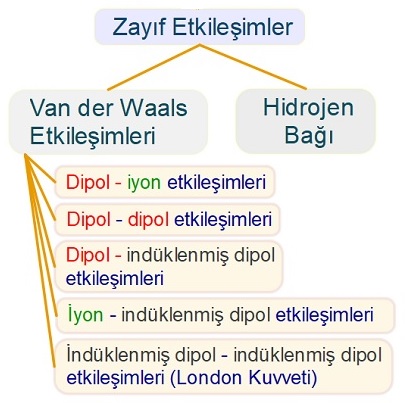
Hangi Kimyasal Türler Hangi Zayıf Etkileşimi Kurar?
Önce Hidrojen Bağı Aranır
Hidrojen bağı şu şartlar altında kurulur:
- F, O, veya N ile kovalent bağ kurmuş H atomu ile diğer molekülün F, O veya N atomları arasında H bağı kurulur.
- İyonlar ve apolar moleküller hidrojen bağı kuramaz.
Hidrojen bağı kurabilen maddeler birbirinde iyi çözünür.
Örnek:
Amonyak çözeltisinde (NH3(suda)) hidrojen bağları:

Hangi Kimyasal Türler Hangi Zayıf Etkileşimi Kurar?
Hidrojen Bağı Yoksa Van der Walls Etkileşimleri Aranır
Van der Waals etkileşimleri şu şartlar altında kurulur:
- Polar moleküller: Dipol etkileşimi kurarlar.
- Apolar moleküller: İndüklenmiş dipol etkileşimi kurarlar.
- İyonlar: İyon etkileşimi kurarlar.
Örnek:
- X polar bir moleküldür.
- Y apolar bir moleküldür.
- Z+2 ise bir iyondur.
Buna göre bu kimyasal türler arasında kurulacak olan Van der Waals etkileşimleri karşılarına yazınız.
- X ile Y arasında :
- Y ile Y arasında :
- Z+2 ile Y arasında :
- X ile X arasında :
- X ile Z+2 arasında :
Çözücü-Çözünen Etkileşimleri
Örnek:
- Asitler, bazlar ve tuzlar suda iyonlarına ayrışarak çözünür.
- Bu tür çözeltilerde iyon-dipol etkileşimleri kurulur.
- NaCl çözeltisindeki (NaCl(suda)) iyon-dipol etkileşimleri:

Örnek:
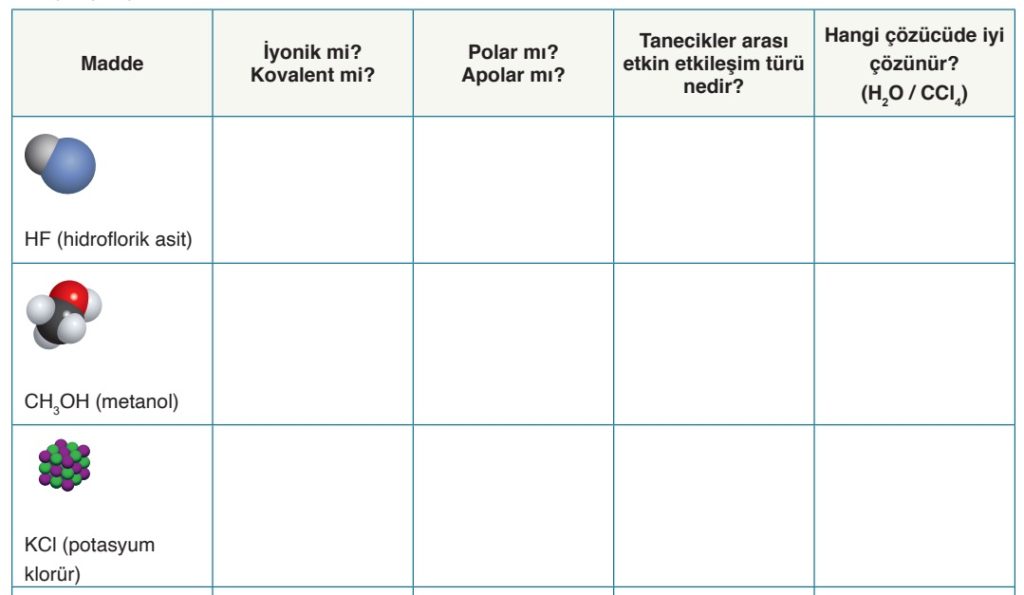
Örnek:
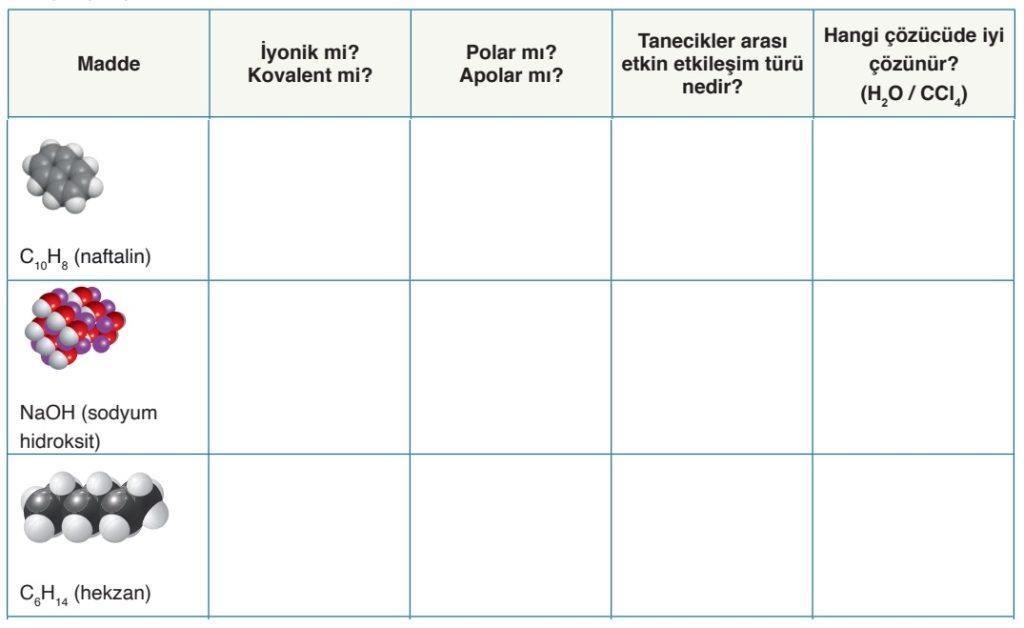
Çözücü-Çözünen Etkileşimleri
Örnek:
Aşağıdaki işlemlerin hangisinde çözünme olmaz?
A) Çaya şeker katılması
B) Suya kolonya damlatılması
C) Yağ damlasının benzinle temizlemesi
D) Suya buz katılması
E) Gazoz yapımında basınçlı gaz kullanılması
Örnek:
“Su ile hidrojen bağı yapabilen maddeler suda daha iyi çözünürler.”
Buna göre aşağıdaki maddelerden hangisi suda diğerlerine göre daha iyi çözünür?
A) CS2
B) CH4
C) C6H6
D) H2S
E) C2H5OH
Örnek:
Aşağıda bileşimi verilen çözeltilerden hangisinde çözücü ile çözünen arasındaki etkileşim yanlıştır?
Çözücü Çözünen Etkileşim
A) H2O NaCl İyon-dipol
B) H2O HF Hidrojen bağı
C) CCl4 CO2 London
D) H2O H2S Dipol-dipol
E) H2O CH4 Hidrojen bağı

2.1. Çözünme Süreci
2.1.2. Maddelerin Birbiri İçindeki Çözünebilirliği
Bitti 🙁