ETKİLEŞİM (KİMYA 10) → 2. Bölüm
DERS
KİMYA 10
1. TEMA:
ETKİLEŞİM
KONU
1.2. Gazlar
1.2.4. Graham Difüzyon ve Efüzyon Yasası
Gazlarda Kinetik Teori
Efüzyon (Püskürme) Nedir?
- Sıkışmış gaz moleküllerinin bulundukları kabın bir bölmesinden diğerine küçük bir delikten geçerek yayılmasına efüzyon (püskürme, dışa yayılma, sızma) adı verilir.
- Efüzyonu basınçlı bir gazın dışarı püskürmesi olarak düşünebiliriz.

Gazlarda Kinetik Teori
Difüzyon Nedir?
- Aynı ortama bırakılan gazların, daha yoğun oldukları taraftan, daha az yoğun olduğu tarafa doğru kendiliğinden akmasına difüzyon denir.
- Difüzyon sonucunda, gazlar homojen bir karışım oluştururlar.
Gazlarda Kinetik Teori
Efüzyon Uygulamaları
- Kütle spektrometrisinde iyonları kütle-yük oranlarına göre ayırmak ve analiz etmek için kullanılır.
- Vakum teknolojisinde, gazların kontrollü bir şekilde ortamdan uzaklaştırılmasını ve vakumun korunmasını sağlar.
- Yarı iletken dağılımı, kontrollü efüzyon süreçleri kullanılarak ince filmlerin alt tabakalara biriktirilmesi esasına dayanır.
Difüzyon Uygulamaları
- Gazların ve besin ögelerinin hücre zarlarından geçişini sağlar.
- İlaçların vücutta belirli bir hızda salınımını sağlamak için kullanılır.
- Gaz karışımlarının ayrılması veya sıvı karışımların saflaştırılması işlemlerinde kullanılır.
Gazlarda Kinetik Teori
Gazların Difüzyonu (Graham Difüzyon Kanunu)
- Mol ağırlığı daha büyük olan gazlar daha yavaş yayılır. (Şişmanlar yavaş koşar.)
- Sıcaklık arttıkça yayılma hızı da artar.
Graham Difüzyon Kanunu
Deneyin Aslını İzleyelim:
Deneyin açıklaması:
Yukarıdaki vidyoda, pamuklara emdirilmiş NH3 (amonyak) ve HCl (hidrojen klorür) sıvılarının buharlarının hızı canlandırılmıştır. NH3 bileşiğinin Mol Ağırlığı 17, HCl bileşiğinin mol ağırlığı ise 36,5’tir. Yani HCl molekülleri daha ağır yani daha yavaştır.
Cam bir borunun iki ucundan aynı anda yola çıkan HCl ve NH3 moleküllerinin karşılaşma noktaları, oluşturdukları NH4Cl (Amonyum klorür) tuzundan anlaşılabilir. Çünkü bu iki madde, bir araya geldiğinde hızlı bir şekilde NH4Cl tuzunu oluşturur. NH4Cl tuzu katı halde bir maddedir.
Vidyoda da görüldüğü gibi, NH3 daha hızlı bir molekül olduğu için iki gazın karşılaşması, HCl emmiş pamuğa daha yakın bir yerde gerçekleşecektir.
Örnek:

Yukarıdaki şekilde, aralarında bir cam boru olan iki cam balonda, aynı koşullarda, He ve SO2 gazları bulunmaktadır. M1 ve M2 muslukları arasında görünen bölmeler eşit uzunluktadır.
Gazların muslukları aynı anda açıldığında, buluşma noktaları için ne söylenebilir? (He: 4 g/mol, SO2: 64 g/mol)
Gazlarda Kinetik Teori
Örnek:
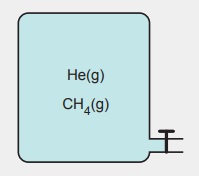
Yukarıdaki şekilde, aynı kabın içinde, eşit mol sayıda He ve CH4 gazları bulunmaktadır. Gazların toplam basıncı, dış basınçtan daha yüksektir. Bu şartlarda, kabın musluğu, kısa bir süre için açılıp kapatılıyor.
Buna göre, aşağıdaki yargılardan hangisi yanlıştır? (He: 4 g/mol, CH4: 16 g/mol)
A) Kaptan dışarıya akan He gazının mol sayısı, CH4 gazından daha çoktur.
B) Kapta kalan He gazının yaptığı basınç, CH4 gazından daha fazladır.
C) Kaptan boşalan CH4 molekülünün sayısı daha azdır.
D) Kaptaki gazların ortalama kinetik enerjileri eşittir.
E) He gazının kimyasal türleri, CH4 gazınınkilerden daha hızlıdır.
Gazlarda Kinetik Teori
Örnek:
Bir gezegenin atmosferinde kükürt hekzaflorür (SF6) gazı bulunduğunu düşününüz. Bu gaz, havadan yaklaşık 6 kat daha ağır bir gazdır.
Buna göre bu gezegende bir konser düzenlenirse sesler Dünya’ya göre nasıl duyulur? Açıklayınız.
Daha Ağır Gazlarda Sesin Yayılması
Kükürt heksaflorür (SF6) gazı ile dolu bir odada olduğunuzu hayal etmek, fiziksel yasaların eğlenceli (ve biraz tuhaf) sonuçlarını görmek demektir. Bu gaz, havadan yaklaşık 6 kat daha yoğun olmasıyla bilinir ve bu yoğunluk sesin davranışını kökten değiştirir.
İşte SF6 atmosferinde sesin başına gelecekler:
1. Ses Hızı Önemli Ölçüde Yavaşlar
Ses hızı, içinden geçtiği ortamın yoğunluğuna ve elastikiyetine bağlıdır.
- Havada ses hızı yaklaşık 343 m/s iken,
- SF6 içinde bu hız yaklaşık 130-150 m/s civarına düşer.
- Neden? SF6 molekülleri, hava moleküllerinden (azot ve oksijen) çok daha ağır ve hantaldır. Ses dalgalarının bu ağır molekülleri hareket ettirmesi daha fazla enerji gerektirir ve dalga daha yavaş ilerler.
2. Sesin Perdesi: “Anti-Helyum” Etkisi
Helyum çektiğinizde sesinizin neden ince çıktığını biliyorsunuzdur; SF6 tam tersini yapar. Eğer bu gazı soluyup (lütfen denemeyin, boğulma riski vardır!) konuşursanız, sesiniz devasa bir canavarınki gibi derin ve kalın çıkar.
- Mekanizma: Ses tellerinizin titreşim frekansı değişmez, ancak ağız ve boğaz yolundaki ses dalgalarının hızı yavaşladığı için rezonans frekansları düşer. Bu da sesin çok daha bas duyulmasına neden olur.
3. Sesin Zayıflaması (Absorsiyon)
SF6 sesi havadan çok daha fazla absorbe eder (emer). Büyük bir SF6 bulutu içinde uzaktaki bir arkadaşınıza seslenirseniz, sesiniz havaya kıyasla çok daha kısa mesafede sönümlenecektir.
- Akustik Empedans: Gazın yüksek yoğunluğu, ses kaynağı (örneğin bir hoparlör) ile ortam arasındaki enerji transferini zorlaştırır.
Gazlarda Kinetik Teori
Örnek:
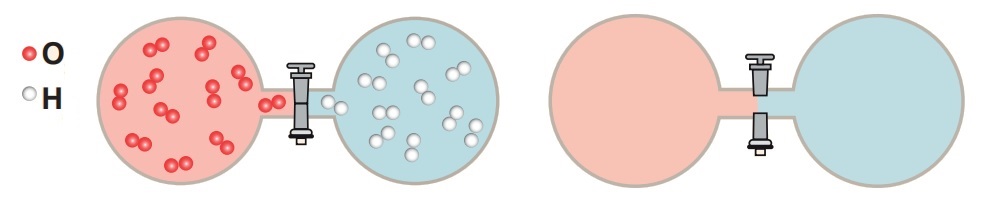
Yukarıdaki kaplarda H2 ve O2 gazları bulunmaktadır. Musluk açılarak gazların difüzyona uğraması için bir süre bekleniyor.
Musluğun açılmasıyla kinetik moleküler teoriye göre gazların yayılımını tanecik modeline dayalı olarak çiziniz.

1.2. Gazlar
1.2.4. Graham Difüzyon ve Efüzyon Yasası
Bitti 🙁